
ミツバチの遺伝解析グループ > 主要業績1
 1.ミツバチへの外来遺伝子導入による遺伝子機能解析法の開発
1.ミツバチへの外来遺伝子導入による遺伝子機能解析法の開発
ミツバチのゲノムプロジェクトが完了した現在、個々の遺伝子の機能を解析する方法論の確立は以前にも増して重要な課題となっています。特定遺伝子の機能は、人為的にその遺伝子の機能を抑制するか、逆にその遺伝子の発現を増強させ、その際に生じる表現型の変化を見ることで調べることができます。しかし、ミツバチではこのような解析を行うための手法が開発されていません。我々はミツバチを分子生物学の新しいモデル動物化すべく、遺伝子機能操作法の開発を行いました。
1RNAi法のミツバチへの応用
特定遺伝子の機能を抑制するために、他の多くの動物で利用されているRNAi法のミツバチへの応用を行いました。RNAi効果を確認するために、標的遺伝子として成虫の肢部形成に関与するdistallessを用いました。ミツバチのdistallessのcDNAを単離し、これをもとにin vitroで2本鎖RNAを合成し、5齢(終齢)幼虫の腹部に注射しました。逆転写定量PCR法でdistalless発現量を測定したところ、注射後12時間ごろからRNA量が有意に減少し、その効果は12日間の蛹期を経て成虫脱皮するまで持続しました。表現型についてみると、2本鎖RNAを注射した実験区の蛹で、肢と口吻が完全に欠失した個体が観察されました。また、成虫に達した個体の44%で一本以上の肢の短縮がみられ、ミツバチでもRNAi法が遺伝子機能抑制法として利用できることが確認されました。他の生物におけるRNAiと同様に、ミツバチでのRNAi効果も完全に遺伝子機能をブロックするものではありませんが、表現型として観察できるレベルの効果があり、形態形成遺伝子に限らず脳内遺伝子等の他の遺伝子機能解析にも応用できると期待されます。
2ミツバチ細胞内で遺伝子発現を促進するプロモーターの検索
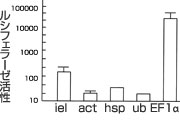
図1 プロモーターアッセイ
各プロモーターにルシフェラーゼ遺伝子をつないだプラスミド(400ng/μl)を産卵後6時間以内のミツバチ卵に顕微注射し、24時間後にルシフェラーゼ活性を測定
3エレクトロポレーション法による脳への遺伝子導入
瞬間的な電気パルスにより遺伝子を細胞に物理的に導入するエレクトロポレーション法により、ミツバチの脳に外来遺伝子を導入できることが、2004年に本COEの外部協力グループにより報告されました(Kunieda & Kubo、2004、Biochem.Biophys.Res.Comm.318、25-31)。
この報告を受け、エレクトロポレーションによる遺伝子導入をより実用的なものとするための改良を試みました。成虫の頭部クチクラの一部を切開して脳を露出させ、脳中央部にCytomegalovirus由来のプロモーターの下流にGreen fluorescent gene(GFP)をつないだプラスミド溶液を注入して、100Vで50ミリ秒の通電と950ミリ秒の非通電を5回繰り返しました。処理個体を33度に設定したインキュベーターで3日間、ショ糖溶液を与えて飼育しました。3日間生存した個体から脳を摘出して蛍光顕微鏡下で観察したところ、陽極電極をあてた付近にGFPのシグナルが観察されました。エレクトロポレーション処理後の生存率は、供試虫の日齢が大きく影響し、若齢のハチを用いることで生存率を格段に上げることができることを見出しました。
4ウイルスベクターによる遺伝子導入
エレクトロポレーション法は簡便ではありますが、物理的外傷が不可避です。そこで個体へのダメージの少ない遺伝子導入法を開発するため、ウイルスベクターの利用を試みました。鱗翅目昆虫由来の核多角体ウイルスは多くの昆虫への遺伝子導入に利用できることが知られており、汎用性の高いウイルスベクターが市販されています。しかし、市販品をそのままミツバチに利用しても良好な結果は得られませんでした。そこで、このウイルスに昆虫DNAウイルスの膜融合タンパク質遺伝子を導入することで、感染率を向上させました。改変ウイルスベクターを成虫(ワーカー)の胸部筋肉および脳に注射し、一過性の遺伝子発現が起こるかどうかを調べ、300個対中半数以上の161個体でGFPの蛍光タンパクの発現を確認しました。
次に多く昆虫でトランスジェニック体作製に利用されているトランスポゾンpiggyBacがミツバチの細胞内でも転移を起こすか検討しました。piggyBacの転移酵素と転移認識部位をそれぞれ別に組み込んだウイルスを作製してミツバチの体細胞中での転移の有無を調べました。転移酵素遺伝子をもつウイルス(ヘルパーウイルス)と、転移させる配列をもつウイルス(ドナーウイルス)を共感染させ10日後に宿主からウイルスDNAを精製し診断PCRをおこなったところ、ドナーウイルスに導入した遺伝子部分が欠損したことを示すPCR産物が増幅され、ミツバチの体細胞中でトランスポゾンが転移活性をもつことが示されました。
トランスジェニック個体の作製には生殖細胞の染色体への導入が不可欠です。女王の腹部にウイルスを注射して10日後に卵巣の組織を取り出してRT-PCRを行い、生殖細胞にウイルスが感染して外来遺伝子が発現することを確認しました。感染女王が産んだ次世代のウイルス伝播率は384個体中2個体と低かったのですが、蛍光顕微鏡下でGFPポジティブな幼虫を選抜して、女王を育てる特別な巣房(王台)に移すことでトランスジェニック女王を作製できると考えられます。
- 【主要業績】1.ミツバチへの外来遺伝子導入による遺伝子機能解析法の開発
- 【主要業績】2.社会刺激依存的に発現量が変化する脳内遺伝子
- 【主要業績】3.概日リズムとピリオド遺伝子
- 研究業績リスト
- グループ研究者紹介