
恄宱寁嶼榑丒岺妛墳梡尋媶僌儖乕僾 > 庡梫嬈愌1
 1丏僔僫僾僗壜慪惈偺儊僇僯僘儉
1丏僔僫僾僗壜慪惈偺儊僇僯僘儉
乣僔僫僾僗丒恄宱嵶朎儗儀儖偺偄偔偮偐偺尰徾傪偮側偖乣
僔僫僾僗壜慪惈偼丄恖娫傗摦暔偵偍偗傞妛廗丒婰壇偺婎慴偱偁傞偲峫偊傜傟偰偄傑偡丅僔僫僾僗慜懁偺揹婥巋寖偵傛偭偰惗偠傞僔僫僾僗壜慪惈偵娭偡傞抦尒偼丄1970擭戙偐傜愊傒廳偹傜傟偰偒傑偟偨丅偙傟傜偺抦尒偐傜丄屻僔僫僾僗偺僗僷僀儞撪僇儖僔僂儉僀僆儞擹搙偵婎偯偔扨弮側尨懃偑僔僫僾僗壜慪惈傪寛掕偟偰偄傞偺偱偼偄偐丄偲偄偆壖愢偑帵嵈偝傟偰偄傑偡丅嵟嬤丄僔僫僾僗慜懁偺巋寖偵壛偊丄僔僫僾僗屻僯儏乕儘儞傕摨帪偵巋寖偟丄椉幰偺僗僷僀僋敪惗帪崗傪徻嵶偵惂屼偟偰丄僔僫僾僗憹嫮丒尭庛偑僔僫僾僗慜屻偺僗僷僀僋僞僀儈儞僌偺弴彉偵埶懚偡傞尰徾偑敪尒偝傟傑偟偨 (Markram et al. 1997; Bi and Poo 1998)丅偙偺尰徾偼丄STDP (Spike-Timing-Dependent synaptic Plasticity, 僗僷僀僋帪崗埶懚僔僫僾僗壜慪惈)偲屇偽傟偰偄傑偡丅STDP偼僗僷僀僋偺憡懳揑僞僀儈儞僌偺傒偱婰弎偱偒傞扨弮側僔僫僾僗壜慪惈儖乕儖傪帵嵈偟偰偍傝丄偙傟傑偱娤應偝傟偰偒偨條乆側忬嫷偱偺僔僫僾僗壜慪惈偺婎慴儖乕儖偲側傞偺偱偼側偄偐丄偲婜懸偝傟傑偟偨丅偟偐偟丄娤應偝傟偨STDP偺僞僀儈儞僌埶懚惈偼丄僇儖僔僂儉擹搙懃偲柕弬偡傞偙偲偑巜揈偝傟偰偄傑偡丅偙偺栤戣傪夝寛偡傞偨傔丄変乆偼僇儖僔僂儉擹搙偵婎偯偔暿偺尨懃傪採埬偟丄娤應偝傟偰偄傞STDP傪嵞尰偟傑偟偨 (Kurashige and Sakai, 2006)丅
僔僫僾僗慜懁偺僗僷僀僋偺屻偵僔僫僾僗屻懁偺僗僷僀僋偑敪惗偟偨偲偒僔僫僾僗偼憹嫮偝傟丄僔僫僾僗屻懁偺僗僷僀僋偺屻偵僔僫僾僗慜懁偺僗僷僀僋偑敪惗偟偨偲偒僔僫僾僗偼尭庛偝傟傑偡(恾B 幚慄)丅椉幰偺僗僷僀僋帪崗偺娫妘傪挿偔偟偰偄偔偲丄僔僫僾僗曄壔偺戝偒偝偼扨挷偵尭彮偟丄悢廫儈儕昩掱搙偱0偵嬤偯偄偰偄偔偙偲偑傢偐偭偰偄傑偡丅
STDP偲屆揟揑側僇儖僔僂儉擹搙懃傪嵞尰偡傞僔僫僾僗壜慪惈偺尨棟偺採埬丅
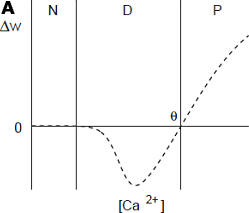
A: 屆揟揑側僇儖僔僂儉擹搙懃丅崅僇儖僔僂儉擹搙偱偼僔僫僾僗憹嫮偑婲偙傝(椞堟P)丄鑷抣兤傛傝掅偄僇儖僔僂儉擹搙偱偼僔僫僾僗尭庛偑婲偙傝(椞堟D)丄偝傜偵掅偄僇儖僔僂儉擹搙偱偼僔僫僾僗嫮搙曄壔偼婲偙傜側偄(椞堟N)丅
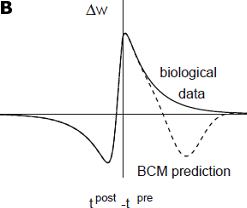
B: 幚尡揑偵娤應偝傟偨STDP偺僞僀儈儞僌埶懚惈(Bi and Poo 1998; Zhang etal. 1998; Feldman 2000; Froemke and Dan 2002)傪掕惈揑偵昤偄偨僌儔僼(幚慄)偲丄屆揟揑側僇儖僔僂儉擹搙懃偐傜梊應偝傟傞僞僀儈儞僌埶懚惈(攋慄)丅
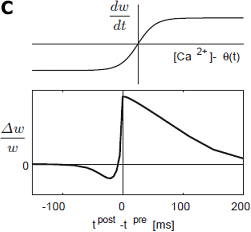
C: 採埬偟偨尨棟偵婎偯偔僔僫僾僗壜慪惈儌僨儖偑帵偡STDP偺僞僀儈儞僌埶懚惈丅
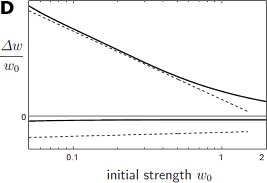
D: 採埬偟偨尨棟偵婎偯偔僔僫僾僗壜慪惈儌僨儖偑帵偡STDP偺弶婜嫮搙埶懚惈(幚慄)偲丄幚尡揑偵娤應偝傟偨弶婜嫮搙埶懚惈(Bi and Poo 1998)傪掕惈揑偵昤偄偨僌儔僼(攋慄)丅
STDP偼乽僇儖僔僂儉擹搙懃乿偵傛偭偰惗偠偰偄傞偲峫偊傜傟偰偒傑偟偨丅乽僇儖僔僂儉擹搙懃乿偲偼丄僔僫僾僗僗僷僀儞撪偵懡検偺僇儖僔僂儉棳擖偑偁偭偨偲偒僔僫僾僗偼憹嫮偝傟(恾A 椞堟P)丄彮検偺僇儖僔僂儉棳擖偑偁偭偨偲偒丄僔僫僾僗偼尭庛偝傟(恾A 椞堟D)丄偝傜偵彮側偄応崌偵偼壗傕曄壔偟側偄(恾A 椞堟N)偲偄偆尨懃偱偡丅僔僫僾僗慜懁偐傜僗僷僀僋偑摓払偟丄僌儖僞儈儞巁偑曻弌偝傟偨屻丄僔僫僾僗屻懁偵妶摦揹埵偑惗偠傞偲丄嵶朎懱偐傜媡揱攄偟偰偒偨妶摦揹埵偑NMDA (N-methyl-D-aspartate) 庴梕懱偐傜偺懡検偺僇儖僔僂儉棳擖傪堷偒婲偙偟丄僔僫僾僗憹嫮偑婲偙傞丅媡偵僔僫僾僗屻懁偵妶摦揹埵偑惗偠偨屻丄僔僫僾僗慜懁偐傜僌儖僞儈儞巁偑曻弌偝傟傞偲丄偦偺偲偒偵偼丄廫暘揹埵偑壓偑偭偨忬懺偵偁傞偨傔丄NMDA庴梕懱偐傜彮検偺僇儖僔僂儉棳擖偟偐婲偙傜偢丄僔僫僾僗尭庛偑婲偙傞丄偲峫偊傜傟偰偄傑偡丅
偟偐偟丄偙偺夝庍偼丄STDP偺僞僀儈儞僌埶懚惈偲堦晹柕弬偡傞偙偲偑巜揈偝傟偰偄傑偡丅僔僫僾僗慜懁僗僷僀僋偺屻僔僫僾僗屻懁僗僷僀僋偑婲偙傞弴斣偺応崌丄僗僷僀僋娫妘傪挿偔偟偰偄偔偲丄僌儖僞儈儞巁偑寢崌偟偨NMDA庴梕懱偺検偑尭偭偰偄偔偨傔丄僇儖僔僂儉棳擖検偼扨挷偵0偵嬤偯偄偰偄偔偼偢偱偡丅偟偨偑偭偰丄昁偢丄僔僫僾僗尭庛偑婲偙傞椞堟(恾A 椞堟D)傪捠夁偡傞偼偢偱丄STDP偺僞僀儈儞僌埶懚惈偵僔僫僾僗尭庛偺椞堟偑偱偒傞偼偢偱偡(恾B 攋慄)丅偟偐偟丄梷惂惈夞楬傪巆偟偨幚尡 (Nishiyama et al. 2000; Tsukada et al. 2005) 埲奜偱偼丄偦傟偵憡摉偡傞傛偆側僔僫僾僗尭庛偼娤應偝傟偰偼偄傑偣傫(Bi and Poo 1998; Zhang et al. 1998; Feldman 2000; Froemke and Dan2002)丅
僗僷僀僋帪崗埶懚僔僫僾僗憹嫮偺戝偒偝偑僗僷僀僋娫妘偲嫟偵扨挷偵0偵尭悐偡傞偙偲傪峫偊傞偲丄廫暘挿偄娫妘偺偲偒偵偼丄僇儖僔僂儉擹搙偑壜慪惈偺婲偙傜側偄掅偄儗儀儖(恾A 椞堟N)偵側偭偰偄傞偺偱偼側偔丄鑷抣兤偵娮偭偰偄傞偺偱偼側偄偱偟傚偆偐丅廫暘偵挿偄僗僷僀僋娫妘偺偲偒偺僇儖僔僂儉擹搙曄摦偼丄僔僫僾僗慜屻偺偦傟偧傟扨敪偺僗僷僀僋偵傛偭偰堷偒婲偙偝傟傞僇儖僔僂儉曄摦偺慄宍榓偵摍偟偔側傞偱偟傚偆丅偟偨偑偭偰丄傕偟丄僔僫僾僗憹嫮偲尭庛偺嫬栚偲側傞鑷抣兤偑曄摦偟偰偍傝丄扨敪偺僗僷僀僋偵傛偭偰堷偒婲偙偝傟傞僇儖僔僂儉曄摦偺慄宍榓偲摍偟偄偲偟偨傜丄捯咫偑偁偆偙偲偵側傝傑偡丅偮傑傝丄偙偺傛偆側曄摦鑷抣兤傪憐掕偡傟偽丄僔僫僾僗慜僗僷僀僋偺屻偵僔僫僾僗屻僗僷僀僋偑敪惗偟偨応崌丄僇儖僔僂儉擹搙忋徃偼NMDA庴梕懱偺惈幙偵傛傝扨敪僗僷僀僋偺応崌偺慄宍榓傪壓夞傞偙偲偼側偔丄寛偟偰僔僫僾僗尭庛偼婲偙傜側偄丄偲偄偆偙偲偵側傝傑偡丅
変乆偼(Kurashige and Sakai, in press)丄偙偺尨棟偵廬偭偨僔僫僾僗壜慪惈儌僨儖傪峔抸偟丄偙偺儌僨儖偑STDP偺僗僷僀僋僞僀儈儞僌埶懚惈傪嵞尰偡傞偙偲傪帵偟傑偟偨(恾C)丅嫽枴怺偄偙偲偵丄偙偺儌僨儖偼丄摿偵弶婜僔僫僾僗嫮搙埶懚惈傪柧帵揑偵摫擖偟偰偄側偄偵傕娭傢傜偢丄幚尡偱娤應偝傟偰偄傞STDP偺弶婜僔僫僾僗嫮搙埶懚惈傪帺摦揑偵嵞尰偡傞偙偲偑傢偐傝傑偟偨(恾D)丅
嶲峫暥專
- Bi G, Poo M (1998) J. Neuroscience, 18:10464-10472.
- Bliss TVP, LAmo T(1973). J. Physiol.(Lond.), 232:331-356.
- Feldman DE.(2000). Neuron, 27:45-56.
- Froemke RC and Dan Y (2002). Nature, 416:433-438.
- Markram H, Lubke J, Frotscher M, Sakmann B.(1997). Science 275:213-215.
- Nishiyama M, Hong K, Mikoshiba K, Poo M.-m, Kato K (2000). Nature, 408:584-588.
- Tsukada M, Aihara T, Kobayashi Y, Shimazaki H (2005). Hippocampus 15:104-109.
- Zhang L, Tao H, Holt C, Harris W, Poo M-m (1998). Nature, 395:37-44.
- 亂庡梫嬈愌亃1丏僔僫僾僗壜慪惈偺儊僇僯僘儉
- 亂庡梫嬈愌亃2丏僔僫僾僗壜慪惈偑恄宱嵶朎偺慖戰惈傗嬊強夞楬偺婡擻偵媦傏偡塭嬁
- 亂庡梫嬈愌亃3丏恄宱嵶朎偺敪壩摿惈偑嬊強夞楬偺嫇摦偵媦傏偡塭嬁
- 亂庡梫嬈愌亃4丏儅僢僠儞僌峴摦偺儊僇僯僘儉
- 尋媶嬈愌儕僗僩
- 僌儖乕僾尋媶幰徯夘